非酒精性脂肪肝是目前最常见的肝脏疾病,全球患病人数近20亿,且发病率呈快速增长趋势。我国非酒精性脂肪肝患病率已超过30%,成为重大公共健康问题和严重社会医疗负担。脂肪肝还是众多心血管疾病、代谢疾病、肿瘤等的重要风险因素,一旦发展到非酒精性脂肪肝炎(以下简称“脂肪肝炎”),将显著增加肝硬化、肝癌、肝衰竭等肝病风险。据统计,脂肪肝炎患者10-15年内发生肝硬化的概率高达15%-25%。因此,脂肪肝炎治疗药物临床需求迫切,预计2030年其全球市场规模将达到350亿美元。
鉴于脂肪肝炎的庞大患病基数、严重健康危害和强烈临床需求,辉瑞、礼来、吉利德、诺和诺德等全球药企加快布局研发该领域新药。目前,全球针对脂肪肝炎的药物试验已有800多项,但没有任何一款药物在美国食品药品监督管理局(FDA)获批进入临床。
乙酰辅酶A羧化酶(ACC)是目前最有潜力的脂肪肝炎治疗靶点,其抑制剂可明显改善肝脏脂肪化、炎症和纤维化,但是已有的ACC抑制剂会导致血脂升高的严重副作用,大大阻碍了其临床应用。
武汉大学李红良教授团队近十年来一直致力于脂肪肝炎等重大临床问题的研究。2021年12月15日,李红良教授团队在国际顶级期刊《科学•转化医学》(Science Translational Medicine)发表两篇题为“Multiple omics study identifies an interspecies conserved driver for nonalcoholic steatohepatitis”和“A small molecule targeting ALOX12-ACC1 ameliorates nonalcoholic steatohepatitis in mice and macaques”的封面文章。这是《科学•转化医学》创刊以来首次背靠背同时发表两篇来自同一研究团队的文章。
该研究揭示了脂肪肝炎发生发展的核心机制,发现12-脂氧合酶(ALOX12)是脂肪肝炎进程的关键靶点,ALOX12可直接靶向ACC1,特异性精准调控ACC1溶酶体降解途径。根据这一发现,李红良教授团队开发出一个全新的小分子化合物,可精准靶向ALOX12-ACC1蛋白相互作用,促进ACC1蛋白降解,显著抑制脂肪肝炎发展。该ALOX12抑制剂的治疗效果显著,而且更重要的是不引起高血脂等副作用。该研究突破性解决了靶向ACC的副作用问题,破解了靶向ACC治疗脂肪肝炎的困境,为ACC抑制剂的开发提供了重要的理论基础,更为靶向ACC治疗脂肪肝炎提出了切实可行的方向。
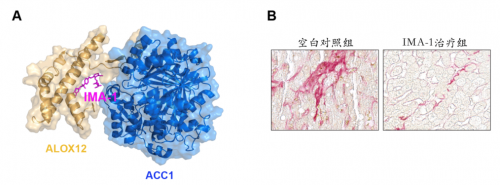
图A. IMA-1抑制ALOX12和ACC1蛋白互作结构图;图B. IMA-1治疗脂肪肝炎效果(红色染色区域代表肝脏纤维化程度)
近年来,李红良教授团队重点围绕ALOX12开展了系列研究,发现ALOX12是肝脏和心脏缺血再灌注损伤的核心驱动因子,明显加重器官炎症和损伤程度;并开发出小分子抑制剂,在小鼠、猪、猴模型中全面证实了靶向ALOX12的小分子药物治疗器官损伤的安全性和有效性。相关研究发表在Nat Medicine (Nat Med. 2018;24:73-83)和Cell Metabolism(Cell Metab. 2021;33:2059-2075.),为提高器官缺血再灌注损伤的预后提供了新的治疗靶点与策略。
ALOX12系列研究工作是李红良教授团队过去十多年来重要代表性研究成果的缩影。李红良教授团队一直聚焦心血管代谢性疾病的发病机制、药物治疗靶点研究和药物研发,系统揭示了心力衰竭、缺血再灌注损伤、非酒精性脂肪肝炎等心血管代谢疾病的作用机制,在 Nat Med、Sci Transl Med、Cell Metab、Circulation、Hepatology、J Hepatol、Nat Commun、PNAS、Hypertension等国际著名期刊上发表相关研究论文200余篇(影响因子大于10的论文100多篇),为脂肪肝病等临床高发心血管代谢性疾病防治提供了重要理论依据。
据了解,《科学•转化医学》杂志是国际著名期刊《科学》(Science)最重要的子刊,最新影响因子17.956。该杂志致力于全球转化医学领域的重大问题研究,发表在该杂志上的原创性研究是疾病预防、诊断或治疗方面的重大突破性进展,填补了基础研究和应用科学结合方面的空白。
免责声明:以上所展示的信息由该企业自行提供,内容的真实性、准确性、合法性由企业负责。一切交易将视为客户自行自愿交易,风险由交易双方负责。本平台对此不承担任何保证责任。如因文章内容、版权和其它问题请与邮箱252425680@qq.com联系删除。